明德生物新冠病毒抗原自测试剂盒,具有快速、便捷、使用场景广泛等特点,15分钟快速获取结果。经德国独立实验室Biomex评估,产品灵敏度96.1%,特异性100%,准确性98%;针对CT值小于30的样本,灵敏度达98.8%,方便个人及家庭对新冠病毒的自主检测。此外,目前已被WHO列为Concern和Interest的8种变异毒株,不影响检测结果。
该产品获取CE自测认证后,不仅能在欧盟31个成员国的EEA内自由流通,直接面向超过5亿人口的消费者市场,更能为全球抗疫增添强援,带来更加便利的检测体验和更加充足的检测资源。
前景广阔 品质无惧考验
随着全球逐步开放,高质量的自测产品将在常态化疫情防控中发挥重要作用。从海外防疫情况来看,新冠抗原自测产品仍具有广阔的市场需求。总的来说,新冠病毒自测产品的全球普及是大势所趋。

△良好易用性彰显国际品质 在获得CE自测认证之前,明德生物新冠病毒抗原检测试剂盒获得了多个权威机构的多重验证:在德国第三方独立检测机构Biomex实验室对抗原产品Clinical performance study和Layperson study中获得极高的测评结果;通过了德国PEI Comparative evaluation、BfArM自测白名单以及英国DHSC Phase 3A validation。
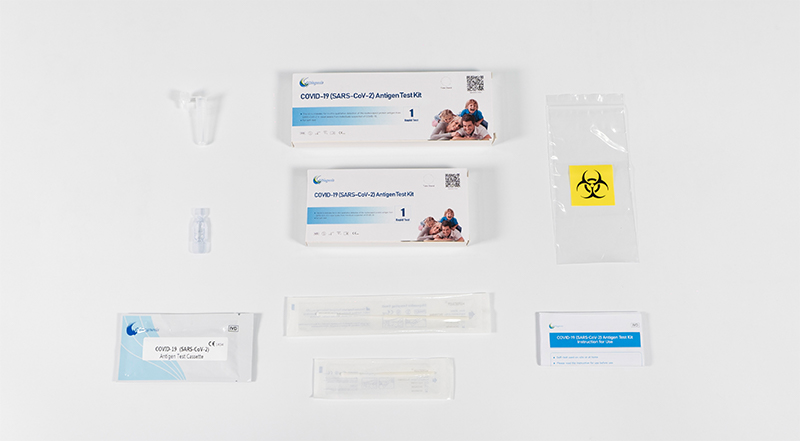
△性能优异,操作方便,使用场景广泛 CE自测认证的加持,再次体现了产品优异性能和良好的用户体验已得到全面认可,满足国际市场需求,也是对明德生物行业影响力、国际客户认同度、国际竞争力的有利佐证。
实时在线 助全球抗疫
目前,明德生物已有18个新冠产品取得了CE准入许可,涵盖新冠核酸、新冠抗体、新冠中和抗体、新冠抗原(专业)、新冠抗原(自测)、新冠变异株核酸检测试剂盒、核酸提取仪、核酸提取试剂等,产品品质得到50多个国家和地区的认可,为全球抗疫贡献明德力量。
14年精工品质,深耕生命健康事业。明德生物以丰富的产品研发、生产、销售及售后经验,沉淀积累了一套完善的质量体系,已开发多款新冠检测试剂,形成了核酸+抗体+抗原产品矩阵和全方位的新冠检测解决方案,满足全球市场各级检测防控需求。
以精益求精的产品,值得信赖的服务团队,助力全球战疫,明德生物始终在线。






 鄂公网安备 42011502000634
鄂公网安备 42011502000634